Mô hình Deep Learning để dự đoán phản ứng miễn dịch trị liệu ở ung thư phổi không phải tế bào nhỏ tiến triển
Mehrdad Rakaee, PhD; Masoud Tafavvoghi, MSc; Biagio Ricciuti, MD; et al
Department of Medicine, Brigham and Women’s Hospital, Harvard Medical School, Boston, Massachusetts
Câu hỏi
Các thuật toán dựa trên Deep Learning có thể sử dụng hình ảnh mô học để dự đoán trực tiếp phản ứng với chất ức chế điểm kiểm soát miễn dịch (immune checkpoint inhibitors ICI) ở những bệnh nhân mắc ung thư phổi không phải tế bào nhỏ (non−small cell lung cancer NSCLC) tiến triển không?
Phát hiện
Nghiên cứu theo dõi này đã phát triển và xác nhận bên ngoài một quy trình tính toán dự đoán phản ứng bao gồm 958 bệnh nhân mắc NSCLC được điều trị bằng liệu pháp đơn trị ICI và chứng minh rằng điểm dự đoán học sâu có liên quan đến tỷ lệ đáp ứng, tỷ lệ sống không tiến triển và tỷ lệ sống tổng thể, với hiệu suất tương đương với phối tử tử vong được lập trình 1 (PD-L1). Kết hợp điểm học sâu và điểm PD-L1 đã cải thiện phân tầng bệnh nhân.
Ý nghĩa
Những phát hiện này chỉ ra rằng một mô hình bệnh lý trí tuệ nhân tạo [artificial intelligence pathology model] có khả năng đóng vai trò là một công cụ mới để hướng dẫn điều trị ICI, tinh chỉnh việc lựa chọn bệnh nhân và cải thiện kết quả lâm sàng trong điều trị NSCLC tiến triển.
Điều trị bằng chất ức chế kiểm soát miễn dịch (ICI) đã mang lại lợi ích lâm sàng cho bệnh nhân ung thư phổi không phải tế bào nhỏ (NSCLC) tiến phát triển hoặc di căn mà không có biến đổi EGFR hoặc ALK, tuy nhiên, chỉ có 25% đến 30% sẽ đáp ứng. Sinh học chỉ điểm dự báo chính của phản ứng với giải pháp đơn trị ICI là biểu hiện phân phối tử vong theo chương trình 1 (PD-L1), một giải pháp không hoàn hảo vì một số bệnh nhân có tài năng PD-L1 thấp có lợi ích từ liệu pháp ICI, trong khi tất cả những người có PD-L1 đều cao đều vào phản ứng. Quản lý Sản phẩm và Dược phẩm Hoa Kỳ đã phê duyệt gánh nặng đột biến khối u có nguồn gốc từ mô hình (TMB) là một sinh học chỉ dự báo cho ICI ở nhiều khối u rắn khác nhau, bao gồm cả NSCLC. Tuy nhiên, việc sử dụng TMB phải đối mặt với các công thức kiểm tra chi phí, tính năng kiểm tra, xác định tối ưu và độ nhạy và đặc tính hạn chế. Do đó, tiếp tục có sự quan trọng trong việc xác định các học sinh điểm bổ sung cho phản ứng miễn phí trị liệu ở những bệnh nhân ung thư giai đoạn tiến phát triển.
ICI phản ứng có thể bị giảm do một số biến thể bộ gen (ví dụ: KEAP1, STK11),11 và có liên quan đến sự bất ổn của vi bảo vệ tinh, tải tân sức kháng nguyên, loại chống hình khối u, tế bào lympho xâm nhập khối u (TIL) và cấu trúc bạch huyết bậc 3 (tertiary lymphoid structures TLS).
Những phát triển gần đây trong trí tuệ nhân tạo đã biến đổi bệnh lý tính toán. Cả thuật toán học máy và học sâu đều được sử dụng để phân tích hình ảnh bệnh lý kỹ thuật số, xử lý các nhiệm vụ như phân đoạn khối u, phân loại, phân nhóm phụ và phân loại tế bào. Trước đây, chúng tôi đã phát triển một số hệ thống phân loại bệnh lý tính toán dựa trên học máy, được thiết kế để xác định kiểu hình miễn dịch,TIL, và TLS bằng cách sử dụng hình ảnh kỹ thuật số mô học tiêu chuẩn. Các dấu ấn sinh học miễn dịch có nguồn gốc từ các quy trình học máy này đã cho thấy mối liên hệ với phản ứng với liệu pháp đơn trị ICI và tỷ lệ sống sót chung ở NSCLC và u hắc tố. Ngoài ra, chúng còn liên quan đến nguy cơ tái phát ở ung thư phổi giai đoạn đầu.
Các mô hình Deep Learning đã được một số nhóm phát triển để diễn giải các mô hình không gian phức tạp trong hình ảnh mô học và dự đoán các yếu tố như sự sống sót và biến đổi bộ gen, ở mức độ tinh vi vượt xa hầu hết các chuyên gia. Khả năng Deep Learning để phân tích đầy đủ các đặc điểm hình ảnh, mà không có ràng buộc hoặc thiên vị trước đó, cho phép đánh giá toàn diện nhiều mô hình bệnh học, có khả năng dẫn đến dự đoán chính xác hơn về kết quả lâm sàng.
Mở rộng những nỗ lực này, các tác giả đã tìm cách phát triển một mô hình phân tầng phản ứng dựa trên học sâu để dự đoán trực tiếp hiệu quả ICI từ hình ảnh kỹ thuật số của các mẫu bệnh lý ở những bệnh nhân mắc NSCLC tiến triển. Nhóm đặt mục tiêu xác thực bên ngoài mô hình trong một nhóm độc lập lớn và so sánh kết quả đầu ra của nó với mức PD-L1, TMB và TIL để dự đoán đáp ứng với điều trị ICI.
Tầm quan trọng
Chỉ một phần nhỏ bệnh nhân ung thư phổi không phải tế bào nhỏ (NSCLC) tiến triển đáp ứng với điều trị bằng thuốc ức chế điểm kiểm soát miễn dịch (ICI). Để có dịch vụ chăm sóc NSCLC cá nhân hóa tối ưu, điều bắt buộc là phải xác định những bệnh nhân có nhiều khả năng được hưởng lợi từ liệu pháp miễn dịch.
Thiết kế, Bối cảnh và Người tham gia
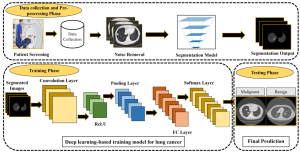
Nghiên cứu nhóm đa trung tâm này đã phát triển và xác nhận độc lập một mô hình phân tầng phản ứng dựa trên học sâu để dự đoán kết quả điều trị ICI ở những bệnh nhân mắc NSCLC tiến triển từ hình ảnh nhuộm hematoxylin và eosin toàn bộ tiêu bản. Hình ảnh để phát triển và xác nhận mô hình được lấy từ 1 trung tâm tham gia tại Hoa Kỳ và 3 trung tâm tại Liên minh Châu Âu (EU) từ tháng 8 năm 2014 đến tháng 12 năm 2022. Phân tích dữ liệu được thực hiện từ tháng 9 năm 2022 đến tháng 5 năm 2024.
Liệu pháp đơn trị với ICI.
Kết quả và Đo lường Chính
Hiệu suất mô hình được đo bằng các điểm cuối lâm sàng và sức mạnh biệt hóa tỷ lệ đáp ứng khách quan (ORR) so với các dấu ấn sinh học dự đoán khác, tức là phối tử chết theo chương trình 1 (PD-L1), gánh nặng đột biến khối u (tumor mutational burden TMB) và tế bào lympho xâm nhập khối u (tumor-infiltrating lymphocytes TIL)
Kết quả
Tổng cộng có 295.581 ô hình ảnh từ 958 bệnh nhân (tuổi trung bình [SD], 66,0 [10,6] năm; 456 [48%] nữ và 502 [52%] nam) được điều trị bằng ICI cho NSCLC đã được đưa vào phân tích.
Nhóm phát triển có trụ sở tại Hoa Kỳ bao gồm 614 bệnh nhân với thời gian theo dõi trung bình (IQR) là 54,5 (38,2-68,1) tháng và nhóm xác nhận có trụ sở tại EU, 344 bệnh nhân với 43,3 (27,4-53,9) tháng theo dõi. ORR đối với ICI là 26% ở nhóm phát triển và 28% ở nhóm xác nhận. Diện tích mô hình học sâu dưới đường cong đặc trưng hoạt động của máy thu (AUC) đối với ORR là 0,75 (95% CI, 0,64-0,85) trong tập kiểm tra nội bộ và 0,66 (95% CI, 0,60-0,72) trong nhóm xác thực. Trong phân tích đa biến, điểm số của mô hình Deep Learning là một yếu tố dự báo độc lập về phản ứng ICI trong nhóm xác thực đối với cả tình trạng không tiến triển (tỷ lệ nguy cơ, 0,56; 95% CI, 0,42-0,76; P < 0,001) và tỷ lệ sống sót chung (tỷ lệ nguy cơ, 0,53; 95% CI, 0,39-0,73; P < 0,001). Mô hình DL được điều chỉnh đạt được AUC cao hơn TMB, TIL và PD-L1 trong tập nội bộ; trong nhóm xác nhận, nó vượt trội hơn TIL và tương đương với PD-L1 (AUC, 0,67; 95% CI, 0,60-0,74), với cải thiện 10 phần trăm về độ đặc hiệu.
Trong nhóm xác thực, việc kết hợp mô hình DL với điểm PD-L1 đạt được AUC là 0,70 (95% CI, 0,63-0,76), vượt trội hơn bất kỳ dấu hiệu nào riêng lẻ, với tỷ lệ đáp ứng là 51% so với 41% đối với riêng PD-L1 (≥50%).
Kết luận và tính liên quan
Tóm lại, mô hình học sâu có khả năng dự đoán phản ứng ICI trực tiếp từ một hình ảnh duy nhất của một phiến nhuộm H&E. Phân tích này có thể đóng vai trò là một dấu ấn sinh học bổ trợ cùng với miễn dịch mô hóa học PD-L1 đối với NSCLC tiến triển, có khả năng tăng cường phân tầng bệnh nhân và cải thiện việc lựa chọn liệu pháp phù hợp cho từng bệnh nhân trong khi tối ưu hóa sự cân bằng lợi ích-chi phí trong điều trị ICI. Việc xác nhận thêm về tiện ích lâm sàng của Deep-IO hoặc một phương pháp tương tự để dự đoán phản ứng với các phác đồ điều trị khác nhau ở NSCLC sẽ rất đáng quan tâm. Những phát hiện của nghiên cứu nhóm này chứng minh một tính năng mạnh mẽ và độc lập dựa trên Deep Learning liên quan đến phản ứng ICI ở những bệnh nhân mắc NSCLC trên nhiều nhóm khác nhau. Việc sử dụng lâm sàng mô hình DL này có thể cải thiện độ chính xác của phương pháp điều trị và xác định tốt hơn những bệnh nhân có khả năng được hưởng lợi từ ICI để điều trị NSCLC tiến triển.
Hạn chế
Nghiên cứu của chúng tôi là bằng chứng tạo ra giả thuyết về nguyên tắc điều tra, và do đó, nó có những hạn chế.
Đầu tiên, dữ liệu về PD-L1 và TMB không có sẵn đồng đều trên tất cả các mẫu, điều này có thể gây ra sai lệch liên quan đến hiệu suất thực tế của các yếu tố này so với Deep-IO.
Thứ hai, tuyến được phát triển không hoàn toàn tự động vì nó yêu cầu đánh giá bệnh lý học về vùng quan tâm trên mỗi slide. Mặc dù bước này hiện là cần thiết, nhưng việc phát triển các phương pháp tự động có thể nâng cao khả năng tái tạo và khả năng mở rộng.
Thứ ba, trong khi mô hình của chúng tôi chứng minh được mối liên hệ với phản ứng ICI, thì nó vẫn chưa đạt ngưỡng AUC lý tưởng là hơn 0,8.
Việc tinh chỉnh thêm, chẳng hạn như sử dụng máy biến đổi thị giác hoặc mô hình đa phương thức, có khả năng cải thiện độ chính xác của nó. Thứ tư, nghiên cứu của chúng tôi chỉ tập trung vào liệu pháp đơn trị ICI, mặc dù có nhiều phương pháp điều trị tuyến đầu đã được chấp thuận kết hợp hóa trị liệu (chemo-ICI). Nghiên cứu sâu hơn có thể khám phá phân tích dựa trên trí tuệ nhân tạo để xác định các đặc điểm tương ứng với phản ứng với liệu pháp chemo-ICI; cũng như hỗ trợ xác định bệnh nhân nào có khả năng được hưởng lợi từ điều trị ICI hoặc chemo-ICI bổ trợ hoặc tân bổ trợ ở NSCLC giai đoạn đầu.
Trích JAMA Oncol. 2025;11(2):109-118. doi:10.1001/jamaoncol.2024.5356